С ростом числа устойчивых к лекарственным препаратам инфекций и сокращением разработки новых антибиотиков мир мог бы использовать новую стратегию в борьбе со все более коварными бактериями.
Теперь стэнфордские химики сообщают в Журнале Американского химического общества о возможном решении: небольшой молекулярной привязанности, которая помогает обычным антибиотикам проникать и уничтожать их цели.
Прикрепление, известное как r8, помогает направлять антибиотики через внешнюю защиту бактерии и побуждает их там задерживаться, сказала Александра Антоноплис, аспирант по химии и соавтор с аспирантом по химии Сяою Цзан.
Эти проникание и цепкость помогают убить бактерии, такие как метициллин - устойчивый золотистый стафилококк, или MRSA,с которым доктора в противном случае боролись бы длительный период.
Действительно, добавление r8 к ванкомицину, первой линии защиты от MRSA, сделало новый препарат в сотни раз более эффективным, согласно экспериментам, проведенным Антоноплисом, Зангом и их советниками, Линетт Кегельски, адъюнкт-профессором химии в школе гуманитарных и естественных наук, и Полом Вендером, профессором химии Фрэнсиса Бергстрема.
Та же стратегия, по мнению исследователей, могла быть использована и в других препаратах борющихся с инфекциями.
"Вам не нужно изобретать новый препарат. Вам просто нужно решить проблемы с существующими лекарствами”, - сказал Уендер, который также является членом Stanford Bio-X, Стэнфордского института рака и Стэнфордского ChEM-H.
Проблема MRSA
В долгосрочной перспективе новый подход может стать хорошей новостью для должностных лиц общественного здравоохранения, которые боролись с устойчивыми к антибиотикам инфекциями, такими как MRSA.
MRSA, которая часто начинает на коже, причина больше чем половину стационар-родственных инфекций в Азии и Америках, и ведущая причина смерти среди антибиотик-упорных инфекций.
“Это глобальная проблема здоровья, и нам нужны новые стратегии лечения, потому что в связи с появлением бактерий, устойчивых к антибиотикам и ограниченности количество антибиотиков в нашем производстве”, - сказал Cegelski, который также является членом Стэнфордского унимверситета.
Это лечение первой линии, антибиотик ванкомицин, может удержать MRSA от распространения в некоторых случаях, предотвращая развитие новых бактериальных клеточных стенок, тем самым предотвращая размножение бактерий.
Но ванкомицин в значительной степени бесполезен против двух ключевых защитных сил бактерий.
Во-первых, MRSA имеет тенденцию образовывать биопленки - колонии бактерий, внедренных в защитную мембрану, через которую лекарственным препаратам трудно проникнуть.
Во – вторых, бактерии MRSA могут находиться в состоянии покоя в течение длительного времени, в течение которого ванкомицин не работает-это означает, что врачам нужен антибиотик, который может действовать до тех пор, пока бактерии MRSA не начнут просыпаться.
Тактика осады антибиотиками
Решение, по мнению команды Стэнфорда, заключается не в разработке антибиотика с нуля, а скорее в модификации ванкомицина с r8, чтобы помочь ему проникнуть в биопленку и держаться достаточно долго, чтобы атаковать клетки, как только они просыпаются.
Для тестирования ванкомицина с присоединенным r8, получившим название V-r8, команда применила его и ванкомицин против MRSA в свободно плавающем состоянии и в биопленках. Когда бактерии свободно плавали в жидкости, ванкомицин и V-r8 могли убить большинство бактерий. Но в биопленках V-r8 был примерно в 10 раз эффективнее, демонстрируя, что он может проникать в биопленку и убивать бактерии внутри. V-r8 также цеплялся за бактерии MRSA дважды, а также ванкомицин и был значительно более эффективным при входе в клетки MRSA, предполагая, что он может висеть достаточно долго, чтобы убить спящие клетки.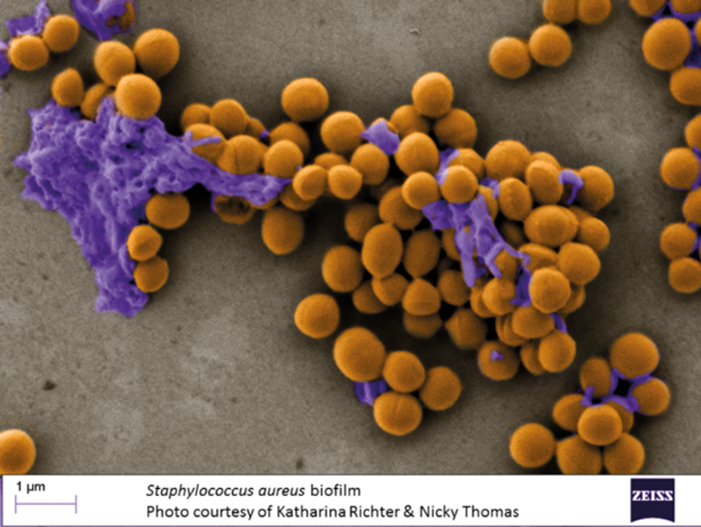
Однако все эти эксперименты проводились в лабораторных условиях. Чтобы увидеть, как V-r8 будет действовать при реальной инфекции, команда лечила мышей, инфицированных MRSA, как V-r8, так и ванкомицином. Новая версия, как они обнаружили, убила около 97 процентов бактерий через пять часов, что примерно в шесть раз эффективнее ванкомицина без вложения r8.
Результаты не означают, что новый антибиотик направляется прямо в клинику, даже для тестирования – это, вероятно, еще годы. Тем не менее, сказал Вендер, они предлагают новый способ создания антибиотиков: путем модификации существующих антибиотиков синтетическими компонентами, чтобы дать им новые способности, такие как способность прорываться через биопленки.
Затем группа намеревается опробовать стратегию модификации лекарств другими бактериями в надежде получить аналогичные результаты и наметить пути решения проблемы устойчивости к антибиотикам.
“Это была просто первая попытка”, - сказал Cegelski.



